Aktuality
Léčba fremanezumabem v měsíčním a kvartálním dávkovacím intervalu s absencí tzv. wearing-off efektu

Migréna představuje neurologické onemocnění, které je spojeno s výraznou disabilitou a zhoršenou kvalitou života. Se zvyšující se frekvencí záchvatů migrén vzrůstá míra negativního dopadu onemocnění na vykonávání každodenních činností. U pacientů se šesti a více záchvaty migrény za měsíc je doporučena profylaktická léčba, při závažném klinickém postižení je indikována ještě při nižším počtu migrenózních dní.
Novou lékovou skupinu v preventivní terapii migrény představují monoklonální protilátky cílící na CGRP (calcitonin gene-related peptide). Tento peptid hraje v patofyziologii migrény klíčovou roli. Anti-CGRP léčba prokázala svoji účinnost ve snižování počtu migrenózních dní. Výhodou oproti stávající preventivní léčbě je specifické působení, dlouhý biologický poločas umožňující dávkování v měsíčních či čtvrtletních intervalech, uspokojivou bezpečnost a snášenlivost léčby a rovněž absenci potřeby postupně titrovat účinnou dávku.
Fremanezumab je plně humanizovaná monoklonální protilátka IgG2, která se selektivně váže na ligand CGRP a blokuje jeho vazbu na receptor. Byla schválena pro použití v klinické praxi ve Spojených státech amerických i v Evropě. Fremanezumab je možné podávat v měsíčním nebo ve čtvrtletním dávkovacím intervalu.
Účinnost a bezpečnost fremanezumabu v léčbě migrény doložila randomizovaná klinická hodnocení fáze III; studie HALO CM u chronické migrény (NCT02621931) a studie HALO EM (NCT02629861) u epizodické migrény [1,2]. Pacienti zařazení v těchto studiích měli následně možnost pokračovat v navazujícím 12měsíčním sledování, do něhož byli zapojeni i další „noví“ pacienti. Výsledky tohoto hodnocení prokázaly, že léčba fremanezumabem je dobře tolerována a poskytuje setrvalou účinnost až po dobu 15 měsíců ve smyslu snížení počtu migrenózních dní za měsíc, počtu dní s migrénou a zmírnění disability spojené s bolestí hlavy [3].
Uvedené klinické studie ukázaly srovnatelný léčebný efekt při dávkování kvartálně i měsíčně.
Při hodnocení pacientů užívajících preventivní léčbu s dlouhým dávkovacím intervalem (onabotulotoxinum A) bylo u některých pacientů pozorováno určité snížení léčebného efektu na konci dávkovacího intervalu [4]. Tento tzv. wearing-off efekt se projevuje návratem nebo zhoršením klinických symptomů před další plánovanou dávkou léku nebo klinickým zlepšením po podání následné dávky. A právě dávkovací interval, resp. účinnost léčby na konci dávkovacího intervalu byla předmětem analýzy, jejíž výsledky přibližujeme.
Metodika hodnocení
Jednalo se o randomizované, dvojitě zaslepené klinické hodnocení fáze III, které zahrnulo 917 a 661 pacientů z původních studií HALO CM a HALO EM [5]. Do sledování bylo zařazeno dalších 312 nových pacientů. Uspořádání studie a časové body hodnocení uvádí obrázek 1.
Obr. 1 Uspořádání klinického sledování a časové body analýzy
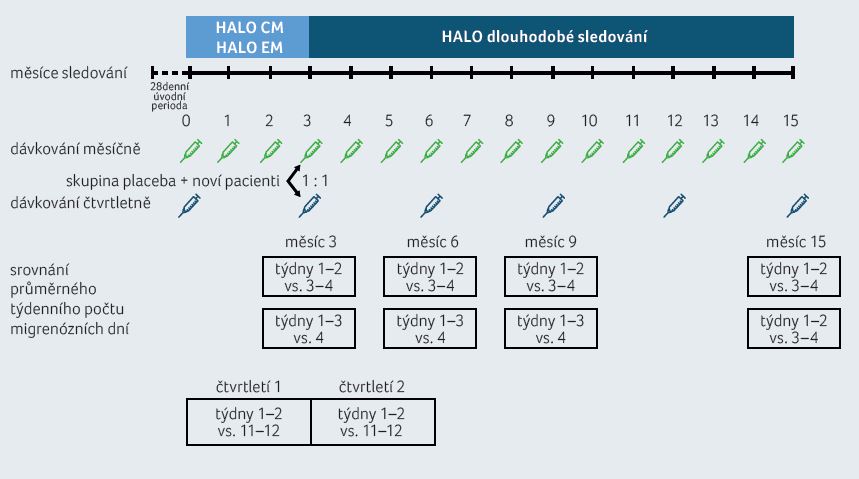 Do hodnocení byli přijímáni pacienti ve věku 18–70 let s anamnézou migrény (dle třetího vydání International Classification of Headache Disorders, ICHD-3) alespoň 12 měsíců před screeningem. Na základě denních záznamů v průběhu 28denní úvodní periody byli pacienti klasifikováni do skupiny s epizodickou (EM) nebo chronickou (CM) migrénou. Za CM byla považována bolest hlavy vyskytující se alespoň 15 dní, z čehož 8 dní splňovalo kritéria migrény dle ICHD-3 beta, pravděpodobné migrény, případně byl podán triptan nebo ergotový derivát. Epizodická migréna byla definována jako bolest hlavy vyskytující se 6–14 dní (pro pacienty z původních studií HALO) nebo 4–14 dní (pro nové pacienty) s minimálně čtyřmi dny, které opět splňovaly daná kritéria ICHD-3. Pacienti mohli pokračovat v dosavadní preventivní léčbě (u původních pacientů maximálně jedna konkomitantní léčba, u nových pacientů dvě medikace) za předpokladu, že byla doložena její alespoň střední účinnost a dávkování bylo stabilní alespoň dva po sobě jdoucí měsíce před screeningem.
Do hodnocení byli přijímáni pacienti ve věku 18–70 let s anamnézou migrény (dle třetího vydání International Classification of Headache Disorders, ICHD-3) alespoň 12 měsíců před screeningem. Na základě denních záznamů v průběhu 28denní úvodní periody byli pacienti klasifikováni do skupiny s epizodickou (EM) nebo chronickou (CM) migrénou. Za CM byla považována bolest hlavy vyskytující se alespoň 15 dní, z čehož 8 dní splňovalo kritéria migrény dle ICHD-3 beta, pravděpodobné migrény, případně byl podán triptan nebo ergotový derivát. Epizodická migréna byla definována jako bolest hlavy vyskytující se 6–14 dní (pro pacienty z původních studií HALO) nebo 4–14 dní (pro nové pacienty) s minimálně čtyřmi dny, které opět splňovaly daná kritéria ICHD-3. Pacienti mohli pokračovat v dosavadní preventivní léčbě (u původních pacientů maximálně jedna konkomitantní léčba, u nových pacientů dvě medikace) za předpokladu, že byla doložena její alespoň střední účinnost a dávkování bylo stabilní alespoň dva po sobě jdoucí měsíce před screeningem.
Pacienti z předchozích placebem kontrolovaných studií HALO CM a HALO EM byli původně randomizováni v poměru 1 : 1 : 1 (do skupiny placeba, k podávání fremanezumabu v dávce 675 mg kvartálně nebo měsíčně, a to u CM v počáteční dávce 675 mg a 225 mg v týdnu 4 a 8, u EM vždy v dávce 225 mg). Pro další sledování byli pacienti z placebové větve randomizováni v poměru 1 : 1 k léčbě fremanezumabem měsíčně nebo kvartálně, stejně tak nově zařazení pacienti. Osoby s původně aktivní léčbou pokračovaly ve stejné medikaci.
Hodnocení
Pro post hoc analýzu byly zaznamenávány průměrné týdenní počty migrénózních dní během týdnů 1–2 a 3–4 v měsících 3, 6, 9 a 15; během týdnů 1–3 a týdne 4 v měsíci 3, 6, 9 a 15; a během týdnů 1–2 a týdnů 11–12 v prvním a druhém čtvrtletí (měsíce 1–3 a měsíce 4–6) léčby (obr. 1). Migrenózní den byl definován jako kalendářní den s minimálně dvěma (EM) nebo čtyřmi (CM) po sobě jdoucími hodinami bolesti hlavy splňující kritéria pro bolest hlavy (migréna s aurou nebo bez aury); v případě pravděpodobné migrény s možnou absencí jednoho kritéria migrény nebo jako den, kdy byla (bez ohledu na délku trvání) použita k léčbě bolesti hlavy akutní antimigrenózní léčba.
Z hlediska bezpečnosti a snášenlivosti léčby byly sledovány nežádoucí účinky a lokální reakce spojené s injekcí (okamžité a do jedné hodiny po injekční aplikaci).
Výsledky
Sledováno bylo celkem 1 890 pacientů (1 110 s CM a 780 s EM). Ze studií HALO pokračovalo 1 578 osob (917 z HALO CM a 661 z HALO EM) a 312 pacientů bylo nově zařazeno (193 s CM a 119 s EM). Z osob převedených ze studií HALO užívalo fremanezumab 611 pacientů ze studie HALO CM (306 pacientů čtvrtletně, 305 pacientů měsíčně) a 432 ze studie HALO EM (217 pacientů čtvrtletně, 215 pacientů měsíčně). Demografické i klinické charakteristiky pacientů byly napříč skupinami srovnatelné. Průměrný věk činil zhruba 44 let, většinu zařazených osob tvořily ženy (přes 84 %) a přibližně čtvrtina pacientů užívala preventivní antimigrenózní medikaci. U pacientů s CM byl průměrný počet dní s migrénou 16,4 (fremanezumab čtvrtletně i měsíčně) a u pacientů s EM 9,2, resp. 9,1 dne (fremanezumab čtvrtletně, resp. měsíčně).
Při hodnocení možného „wearing-off“ efektu v rámci měsíčního intervalu byly srovnávány počty migrenózních dní v první a druhé polovině měsíce a dále jejich počty v prvních třech týdnech oproti poslednímu týdnu měsíce. Zvlášť pro skupinu s CM a EM. Výsledky hodnocení popisují grafy 1A–D a 2A–D. Při mezitýdenním srovnání nebyl zaznamenán rozdíl v týdenním počtu dní s migrénou. Počáteční týdenní počet migrenózních dní u pacientů s CM (na počátku průměrně 4 dny) poklesl během prvních dvou týdnů sledování zhruba o 35 %, ve skupině pacientů s EM (na počátku průměrně 2,3 dne) zhruba na polovinu při obou dávkovacích intervalech. Dosažený pokles přetrval v průběhu dalších hodnocených intervalů.
GRAF 1A–D Srovnání průměrného počtu migrenózních dní mezi týdny 1–2 a 3–4.
grafy A, B – fremanezumab čtvrtletně; grafy C, D – fremanezumab měsíčně
grafy A, C – pacienti s chronickou migrénou; grafy B, D – pacienti s epizodickou migrénou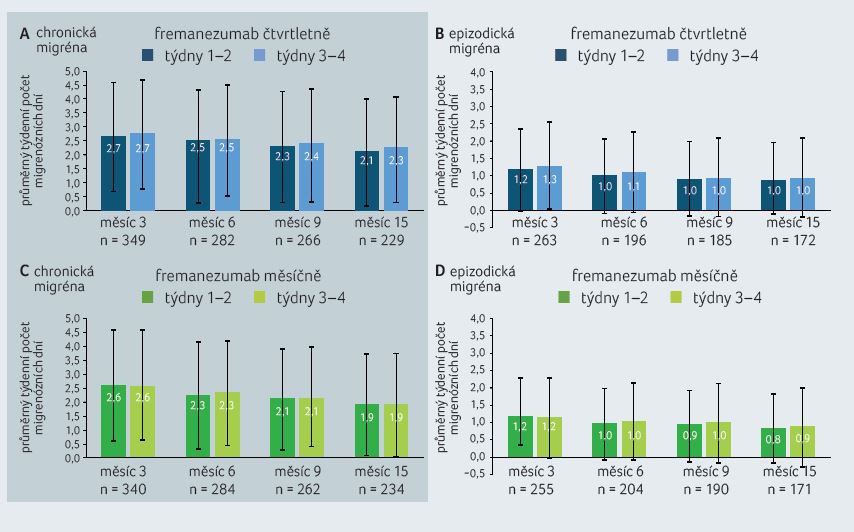
GRAF 2A–D Srovnání průměrného počtu migrenózních dní mezi týdny 1–3 a 4.
grafy A, B – fremanezumab čtvrtletně; grafy C, D – fremanezumab měsíčně
grafy A, C – pacienti s chronickou migrénou; grafy B, D – pacienti s epizodickou migrénou
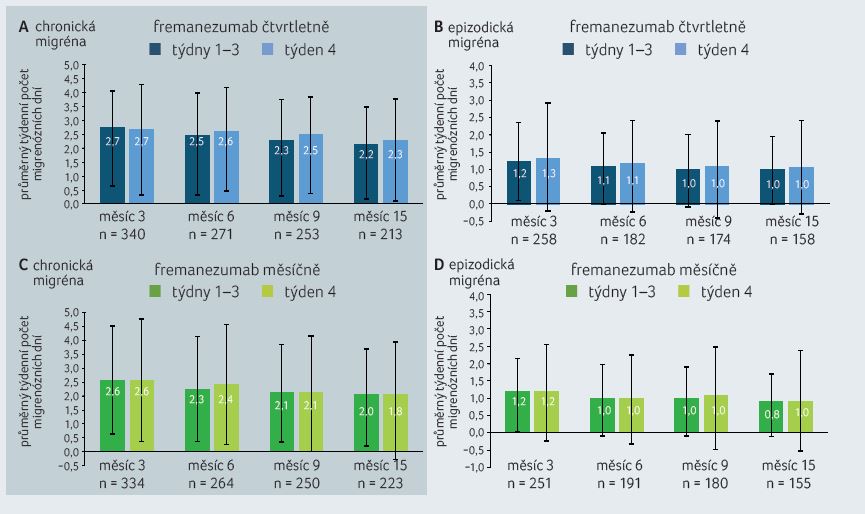
Při analýze týdenního počtu migrenózních dní u pacientů s CM a EM v rámci čtvrtletí nebyl mezi počátečním (týden 1–2) a konečným (týden 11–12) obdobím zaznamenán žádný vzestup při měsíčním i čtvrtletním dávkovacím intervalu. Výsledky sledování přibližuje graf 3A–D.
GRAF 3A–D Srovnání průměrného počtu migrenózních dní mezi týdny 1–2 a 11–12.
grafy A, B – fremanezumab čtvrtletně; grafy C, D – fremanezumab měsíčně
grafy A, C – pacienti s chronickou migrénou; grafy B, D – pacienti s epizodickou migrénou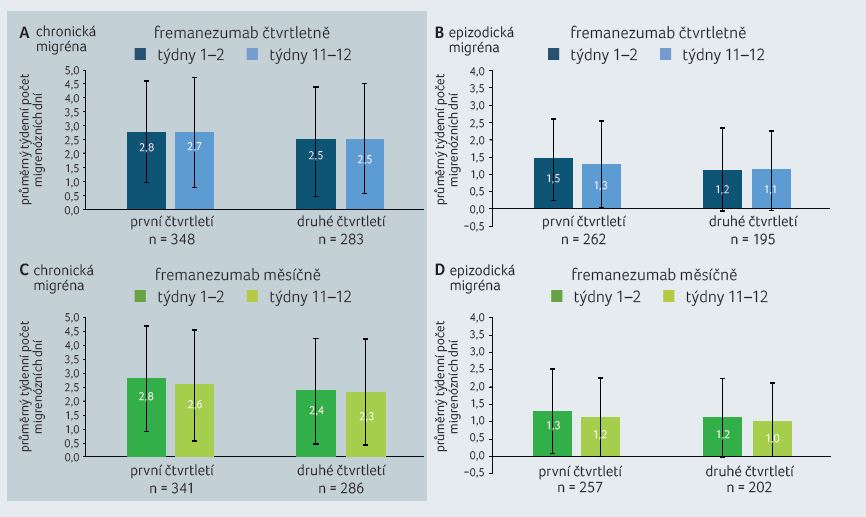 Dlouhodobé klinické hodnocení neopomnělo sledovat bezpečnost a snášenlivost léčby. V souladu s předchozími studiemi byly nejčastěji hlášeným nežádoucím účinkem reakce v místě vpichu (indurace, bolest, erytém) se stejnou frekvencí výskytu ve všech podskupinách pacientů. Závažné nežádoucí účinky vedoucí k přerušení léčby byly vzácné.
Dlouhodobé klinické hodnocení neopomnělo sledovat bezpečnost a snášenlivost léčby. V souladu s předchozími studiemi byly nejčastěji hlášeným nežádoucím účinkem reakce v místě vpichu (indurace, bolest, erytém) se stejnou frekvencí výskytu ve všech podskupinách pacientů. Závažné nežádoucí účinky vedoucí k přerušení léčby byly vzácné.
Shrnutí
Analýza dat dlouhodobého klinického sledování fáze III doložila, že u pacientů léčených fremanezumabem v měsíčním nebo čtvrtletním intervalu nedochází k poklesu účinnosti terapie na konci dávkovacího intervalu (tzv. wearing-off efekt). Účinnost obou forem dávkování fremanezumabu je v souladu s předchozím zjištěním srovnatelná a volbu režimu je možné přizpůsobit individuální potřebě a preferencím pacienta.
Redakčně zpracovala PharmDr. Kateřina Viktorová
Literatura
Silberstein SD, Dodick DW, Bigal ME, et al. Fremanezumab for the preventive treatment of chronic migraine. N Engl J Med 2017; 377: 2113–2122.
Dodick DW, Silberstein SD, Bigal ME, et al. Effect of fremanezumab compared with placebo for prevention of episodic migraine: A randomized clinical trial. JAMA 2018; 319: 1999–2008.
Goadsby PJ, Silberstein SD, Yeung PP, et al. Longterm safety, tolerability, and efficacy of fremanezumab in migraine: A randomized study. Neurology 2020; doi: 10.1212/WNL.00000 00000 010600.
Quintas S, Garcia-Azorin D, Heredia P, et al. Wearing off response to onabotulinumtoxinA in chronic migraine: Analysis in a series of 193 patients. Pain Med 2019; 20: 1815–1821.
Blumenfeld AM, Stevanovic DM, Ortega M, et al. No “Wearing-Off Effect” Seen in Quarterly or Monthly Dosing of Fremanezumab: Subanalysis of a Randomized Long-Term Study. Headache 2020; 60: 2431–2443.
Zdroj: Remedia 2021, roč. 31, č. 1. Dostupné z: http://www.remedia.cz


